三阴性乳腺癌(TNBC)是乳腺癌中最具侵袭性的一种,由于不表达激素受体以及HER2,无法使用靶向治疗,长期以来TNBC患者只能接受手术以及放化疗。
免疫检查点抑制剂疗法的出现为TNBC患者带来了新的希望,然而临床试验发现PD-1抑制剂联合化疗仅能使一小部分TNBC患者获益[1,2]。因此,探究TNBC对免疫检查点抑制剂治疗耐药的机制至关重要,这将为改善免疫治疗效果提供参考。
近期,由Dana-Farber癌症中心Judith Agudo教授领衔的研究团队在Cell期刊发表重要研究成果[3],他们发现在TNBC中有一群抵抗T细胞杀伤的静息肿瘤细胞(QCCs)。这些QCCs通过激活HIF1a,与免疫抑制性成纤维细胞、功能失调的DC细胞一起形成了一个抵御T细胞浸润与杀伤的微环境。从而在免疫治疗中存活下来并引起肿瘤复发。
这项研究成果为我们揭开了乳腺癌免疫逃逸的神秘面纱,突出了QCCs在乳腺癌免疫逃逸中的重要作用,提示我们靶向清除QCCs可能是破解TNBC免疫耐药难题的有效途径。

论文首页截图
以往有研究发现一些基因在肿瘤细胞抵抗免疫治疗中具有一定作用[4,5],但是这些研究并不能解释肿瘤细胞是如何营造出一个免疫抑制性微环境的;此外,通过测序的手段能够找到对免疫检查点抑制剂治疗耐药肿瘤所具备的一些特征,但是肿瘤组织中存在大量异质性的细胞群体,这大大增加了寻找肿瘤耐药机制的难度。例如丢失肿瘤抗原的癌细胞与肿瘤抗原阳性的癌细胞在逃脱免疫系统追杀过程中采取的方法显然是不同的。
在这项研究中,Agudo教授团队希望探究那些表达肿瘤抗原的癌细胞是怎么逃脱免疫系统的追杀的。因此,他们为小鼠接种了表达GFP或mCherry的TNBC细胞系4T07,并为小鼠转输特异性识别GFP的PD-1-/-Jedi T细胞(敲除PD-1是为了模拟PD-1抑制剂治疗)。由于Jedi T细胞的TCR只能特异性识别GFP而不能识别mCherry。因此该实验模型可以用来探究持续表达肿瘤特异性抗原的肿瘤细胞(GFP+肿瘤细胞)是如何逃脱肿瘤抗原特异性T细胞(Jedi T细胞)的攻击。
研究团队在转输Jedi T细胞后第5天分析肿瘤内GFP+与mCherry+肿瘤细胞的比例,发现Jedi T细胞杀死了大部分GFP+肿瘤细胞,但是仍然有一部分GFP+肿瘤细胞逃脱了T细胞的杀伤。免疫荧光染色发现这些逃脱杀伤的GFP+肿瘤细胞形成了一个细胞簇,在细胞簇内部T细胞浸润水平降低了两倍。这说明幸存的GFP+肿瘤细胞簇能够阻止T细胞的浸润,这可能是导致其对免疫治疗产生抵抗的原因之一。
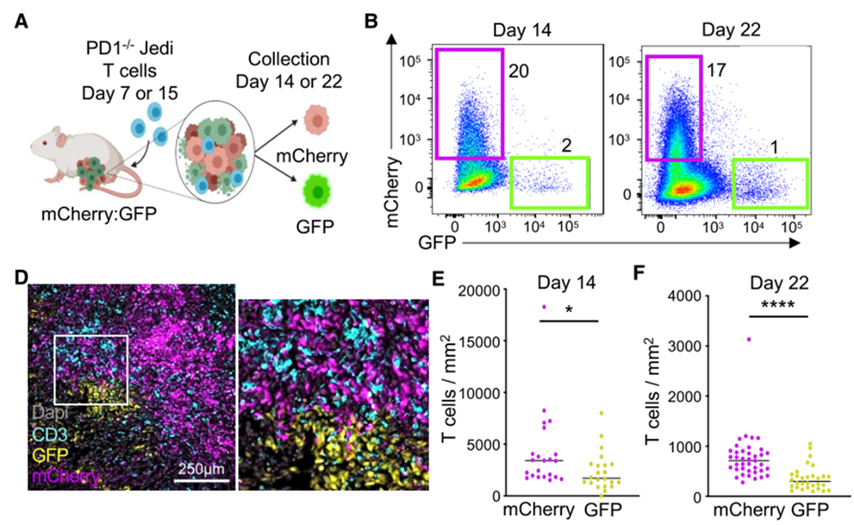
Jedi T细胞攻击后存活的GFP+肿瘤细胞聚集成簇
接下来,Agudo教授团队分析了幸存的GFP+肿瘤细胞与对照mCherry+肿瘤细胞的转录组差异。他们发现,与mCherry+肿瘤细胞相比,GFP+肿瘤细胞中与细胞周期相关的基因明显下调。EdU(胸腺嘧啶核苷类似物5-乙炔-20-脱氧尿苷)掺入实验表明这些在Jedi T细胞攻击后存活的GFP+肿瘤细胞处于细胞周期停滞状态(称为静息肿瘤细胞,QCCs)。
那么这些QCCs是否对T细胞的杀伤更具抗性呢?研究团队向肿瘤细胞中转入tdTomato-p27K,这可以使QCCs被tdTomato标记。向荷瘤小鼠转输PD-1-/- Jedi T细胞后发现,相比于对照非免疫原性miRFP670+肿瘤细胞,存活下来的GFP+肿瘤细胞大部分都是tdTomato+的,这说明QCCs对T细胞的杀伤具有更强的抵抗能力。
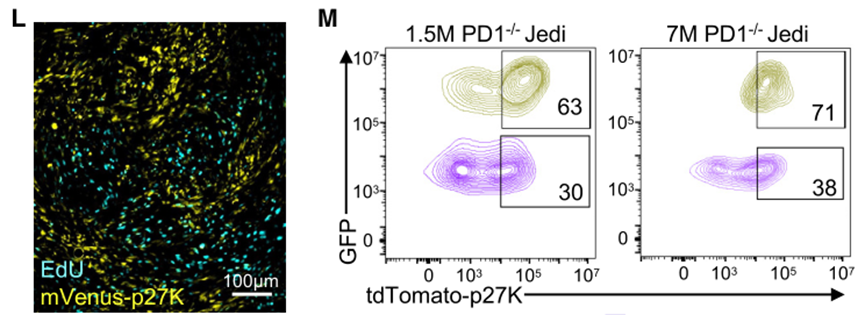
在Jedi T细胞攻击中存活下来的GFP+肿瘤细胞处于细胞周期静息状态,并对T细胞的杀伤具有更强的抵抗力
以上的结果表明在小鼠模型中,QCCs是免疫治疗耐药的主力,那这种现象在人类患者中是否也存在呢?通过分析乳腺癌患者组织病理样本以及转录组测序,研究院队发现,在肿瘤组织中与T细胞接触的肿瘤细胞大多是Ki67+的增殖细胞,p27+的QCCs极少与T细胞接触;同时基因集富集分析表明,与治疗无应答者相比,免疫治疗应答患者的肿瘤细胞在DNA复制相关通路更加富集,表明它们处于非静止状态。这种相关性提示我们,QCCs可能与乳腺癌患者免疫治疗效果不佳有关。
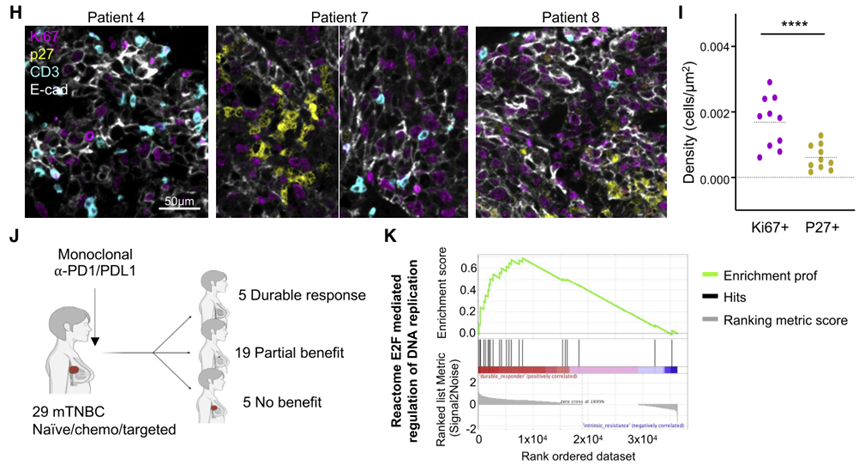
乳腺癌患者肿瘤组织中静息肿瘤细胞周围T细胞浸润较少,并且对免疫治疗有应答的患者其肿瘤细胞处于细胞周期活跃状态
为了探究QCCs的耐药机制,研究团队对QCCs以及非静止肿瘤细胞进行RNA测序。数据分析表明,QCCs上调了缺氧以及葡萄糖代谢相关通路基因。免疫荧光染色结果显示,p27K+QCCs与缺氧探针共定位,而T细胞则很少浸润至缺氧区域;Jedi T细胞治疗后幸存的GFP+肿瘤细胞也位于低氧区域中。这些数据表明乳腺癌中的QCCs主要位于T细胞浸润较少的缺氧微环境中。
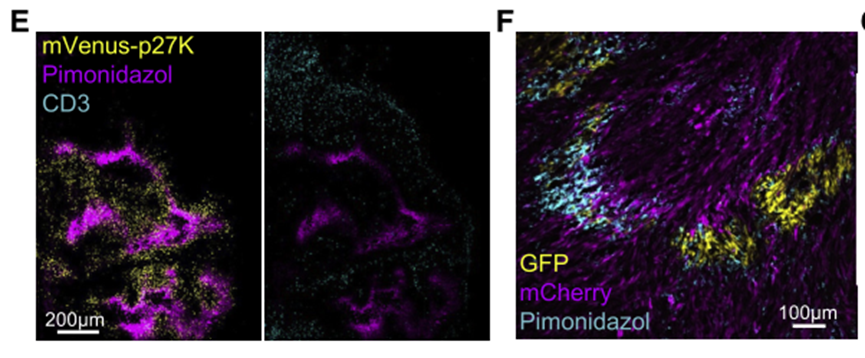
QCCs所在区域处于明显的低氧状态,并且T细胞浸润较少
接下来,为了在单细胞水平上分析QCCs抑制T细胞功能的机制,Agudo教授团队分离了QCCs细胞簇内外的浸润细胞,并对其进行单细胞转录组测序。
通过数据分析发现,QCCs细胞簇内部存在大量免疫抑制性成纤维细胞,这解释了为何QCCs区域浸润T细胞数目较少。
对QCCs细胞簇内外浸润T细胞进行分析发现,浸润在缺氧的QCCs细胞簇内部的CD8+ T细胞耗竭程度更深,杀伤能力更弱。
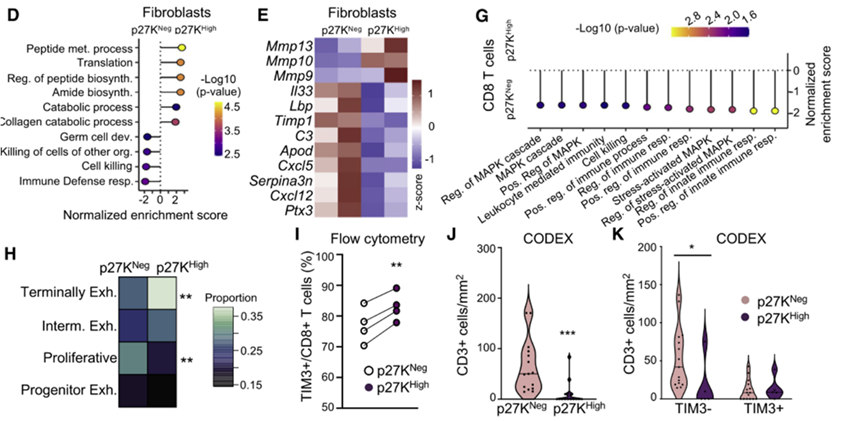
QCCs细胞簇内部存在大量免疫抑制性成纤维细胞,浸润的T细胞数量显著低于QCCs细胞簇外,并且QCCs细胞簇内浸润的T细胞耗竭程度更高
究竟是哪群细胞促进了T细胞的功能失调呢?通过对QCCs内部浸润各细胞亚群进行缺氧特征评分,研究团队发现DC细胞表达丰富的缺氧相关基因,并且下调促进T细胞活化的基因,如MHCⅠ与MHCⅡ、IL-12、CD80/86,表明这些DC细胞促进T细胞活化的能力极大地减弱了,这可能是QCCs细胞簇内部浸润的T细胞功能失调的重要原因。
但是Agudo教授团队通过缺氧诱导实验发现,缺氧并不能直接削弱DC细胞活化T细胞的能力,所以研究团队将目光转向QCCs本身。探究是否是表达HIF1a的QCCs塑造了免疫抑制性的微环境,损伤DC细胞活化T细胞的能力进而抑制了T细胞免疫应答。为此,他们构建了表达活化型HIF1a(HIF1aSTBL)的乳腺癌细胞系。
荷瘤实验显示,相比于WT肿瘤,表达HIF1aSTBL的肿瘤内浸润的T细胞数量更少,耗竭程度更深;瘤内DC细胞上MHCⅡ表达明显下调,这些现象与在QCCs细胞簇内部观察到的基本一致。
更进一步地,研究团队将WT或表达HIF1aSTBL的GFP+肿瘤细胞与mCherry+肿瘤细胞混合接种至小鼠皮下。发现相比于mCherry+: GFP+肿瘤组,接种了mCherry+: GFP+ HIF1aSTBL肿瘤细胞的小鼠瘤内浸润T细胞数量更少,并且T细胞更难接近GFP+肿瘤细胞,存活的GFP+肿瘤细胞的数量增加了数倍,可见HIF1a能够促进肿瘤细胞免疫逃逸。
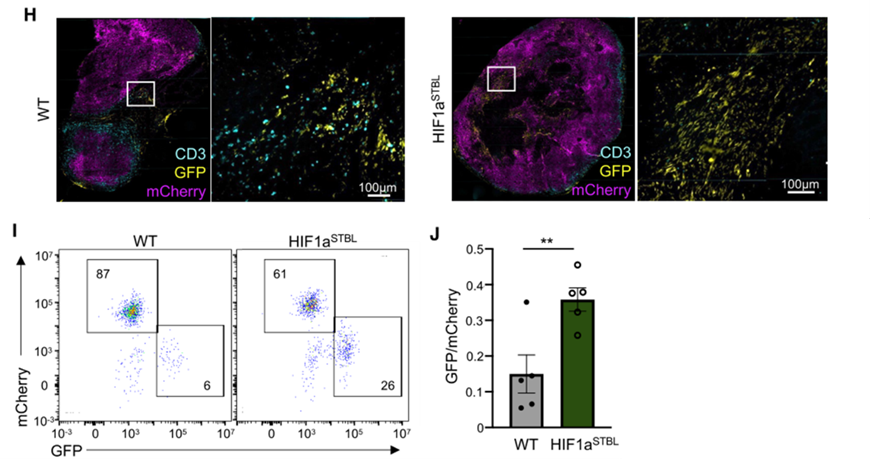
肿瘤细胞过表达HIF1aSTBL后能够抑制T细胞的浸润并逃脱T细胞的攻击
综合以上数据可见,QCCs正是通过高表达HIF1a从而来营造一个免疫抑制性的微环境,逃脱肿瘤抗原特异性CD8+T细胞的追杀。那么敲除肿瘤细胞中的HIF1a是否就能够促进T细胞对肿瘤的杀伤呢?实验结果表明敲除肿瘤细胞中的HIF1a后,肿瘤内浸润T细胞数量显著增加并且耗竭程度降低,肿瘤体积明显减小。这提示我们靶向肿瘤内HIF1a能够促进抗肿瘤免疫应答,抑制肿瘤生长。
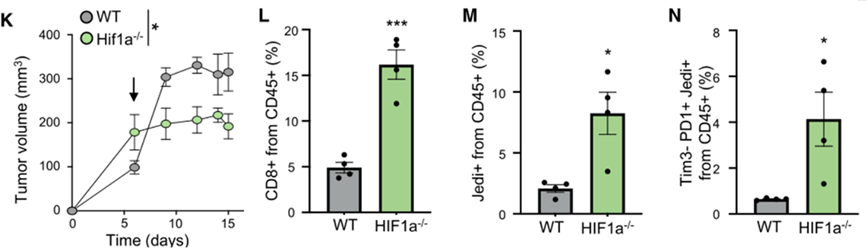
敲除肿瘤细胞中的HIF1a显著增强了抗肿瘤免疫应答
总的来说,这项研究揭示了肿瘤抗原阳性的癌细胞免疫逃逸的机制:它们聚集成团,召唤成纤维细胞为它们筑起屏障;一起进入静息状态并高表达HIF1a,使得免疫系统的哨兵——DC细胞功能失调,进而抑制T细胞免疫应答。这些努力使得它们得以逃脱T细胞的追杀,并在免疫治疗后卷土重来。
同时,这项研究结果也提示我们根除QCCs是改善TNBC免疫治疗效果和预防肿瘤复发的关键。