新冠变异株快速产生,刺突蛋白表面的突变直接影响疫苗和抗体药物的有效性,因此亟需开发针对变异株的疫苗。多价纳米颗粒重组蛋白疫苗具有明显优势,能够诱导更强的体液免疫,将多种突变蛋白表面展示发挥广谱保护作用。
近日,中山大学肿瘤防治中心曾木圣教授课题组与广州医科大学赵金存教授课题组合作,在 Nature Communications 期刊发表了题为:Quadrivalent mosaic HexaPro-bearing nanoparticle vaccine protects against infection of SARS-CoV-2 variants 的研究论文。
该研究开发了一种四价嵌合纳米颗粒疫苗同时展示四种新冠刺突蛋白,能够在动物模型中有效保护不同毒株感染。

研究者将融合前构象的HexaPro连接至三聚体I53-50A的N端,再将五聚体I53-50B.4PT1与HexaPro-I53-50A混合,体外组装成四价嵌合型免疫原,同时研究者也将不同变体HexaPro-I53-50A制成鸡尾酒。
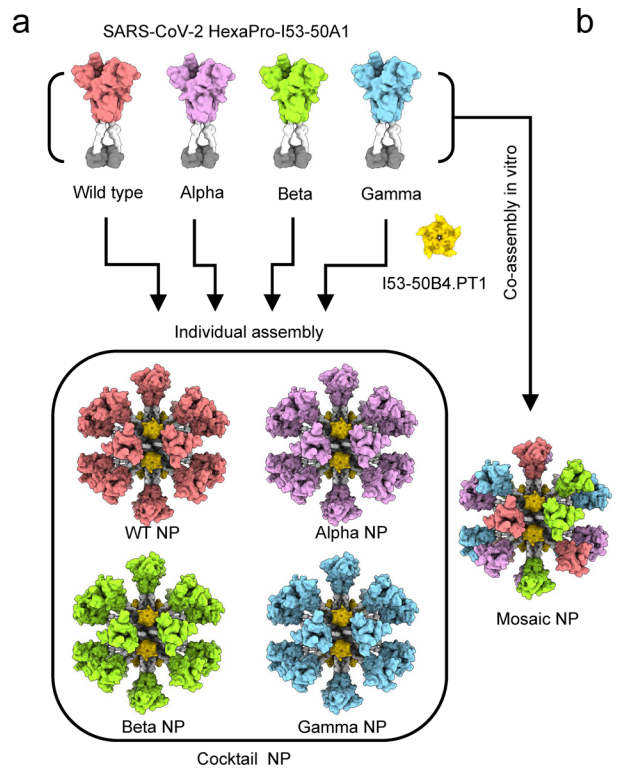
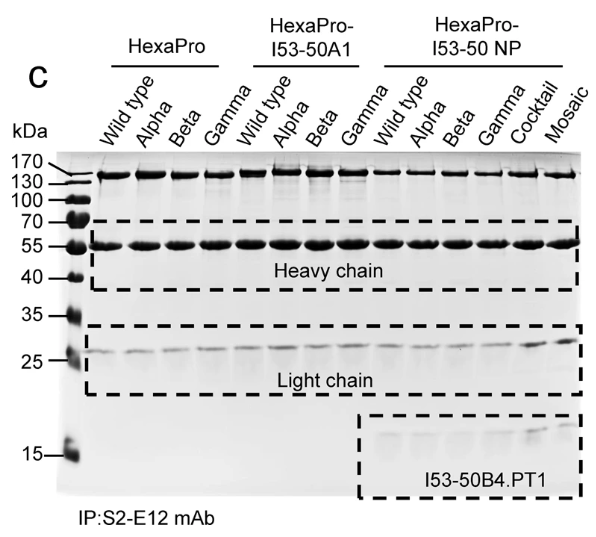
通过电镜负染观察,四价嵌合重组蛋白形成了正二十面体纳米颗粒。免疫沉淀与酶联免疫吸附试验都表明重组蛋白能够被广谱中和抗体识别结合。
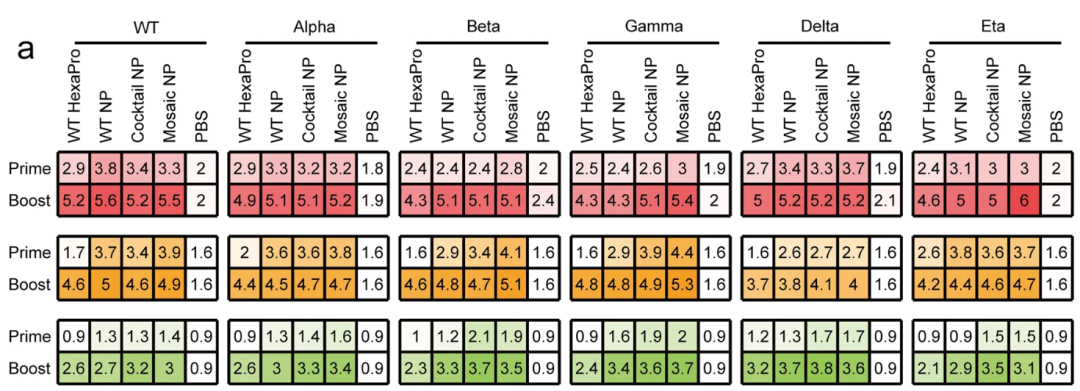
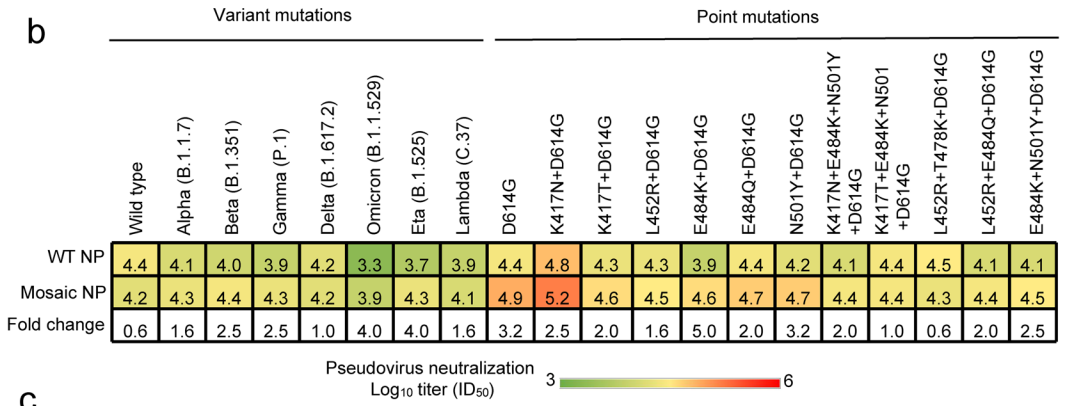
研究者在小鼠模型上评估了嵌合型重组蛋白的保护效果,与野生型Hexpro重组蛋白相比,嵌合型免疫原对新冠变异毒株产生的抗体水平明显更高(2-16倍),抗体谱也更为广泛。血浆病毒中和试验也表明嵌合重组蛋白或鸡尾酒重组蛋白都能够高效激发中和抗体。
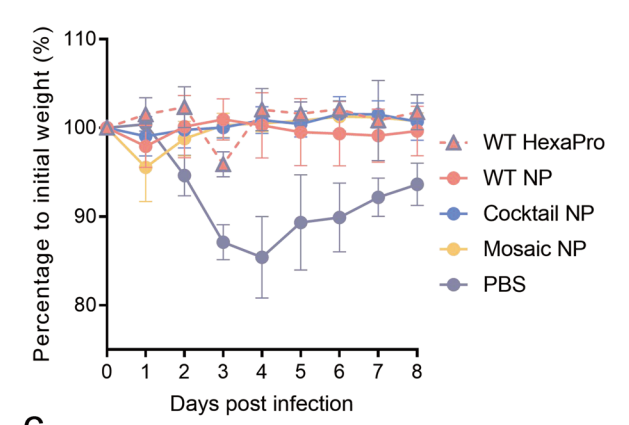
研究者用新冠B.1.351毒株进行了攻毒试验,用重组蛋白刺激产生的血浆治疗小鼠能有效改善肺部病变和系统性炎症,另一方面接种重组蛋白能够预防小鼠感染B.1.351和原始毒株。
研究者也在食蟹猴模型中观察到类似的现象,研究者还对抗体谱进行了测定,Omicron和lambda突变株能够逃逸野生型重组蛋白激发的抗体免疫,而嵌合型重组蛋白激发的抗体水平仅有微弱下降。
该研究为广谱新冠疫苗开发提供了新思路,通过多价展示的方式同时免疫多个毒株刺突蛋白。